Процесс ржавчины металла может застать врасплох в самый неподходящий момент и если помедлить с его предотвращением, то в конце концов безобидное пятно преобразуется в сквозное отверстие. К сожалению, полностью предотвратить появление ржавчины на кузове автомобиля невозможно.
Самым востребованным способом удаления ржавчины по сей день является полная зачистка изделия, грунтовка и последующая окраска.
Но данный способ имеет свои минусы и самый главный из них, это короткий срок действия процедуры. Как правило, все вышеперечисленные манипуляции приходится выполнять регулярно минимум раз в 6 месяцев.
К счастью, на смену данному способу пришла очистка кузова с помощью электролиза. Данная статья поможет разобраться с процессом очистки кузова автомобиля от ржавчины с помощью электрохимического способа.

Причины появления ржавчины
Более научное название процесса ржавчины – коррозия. Коррозия металлов представляет собой разложение железа в следствии окисления, вызванного воздействием на металл воды и кислорода.
Коррозию классифицируют на:
- Электрохимическую. Чаще всего она вызвана избыточной влажностью окружающей среды.
- Химическую. Возникает при взаимодействии металла с каким-либо агрессивным веществом.
- Биокоррозию. В связи с воздействием на металл бактерий и прочих микроорганизмов.

В бытовых условиях, чаще всего металлы подвергаются коррозии из-за несоблюдения условий хранения изделия. Также возможно возникновение ржавчины из-за неправильно подобранного средства для ухода на кузовом машины, например, неправильного моющего средства.

Почему сложно избавиться от коррозии
При взаимодействии железа с водой, на поверхности металла образуется порошок бурого цвета, который, в свою очередь, является катализатором или ускорителем для осуществления процесса коррозии металла.
На начальных стадиях ржавчины, ее зачищают, делается это для того, чтобы убрать большую часть катализатора и приостановить процесс. Но полностью избавиться от образовавшегося порошка невозможно, поэтому ржавчина появляется снова и снова.

Обратите внимание! Несмотря на мгновенный результат, механические способы удаления коррозии являются менее эффективными, потому стоит обратить внимание на химические способы борьбы с коррозией.
Электрохимический способ
Процесс представляет собой восстановление одного химического элемента за счет расщепления другого при контакте друг с другом.
Для того, чтобы осуществить электролиз в домашних условиях понадобится:
- источник тока;
- электролит;
- металл с отличающейся от железа электрохимической активностью.
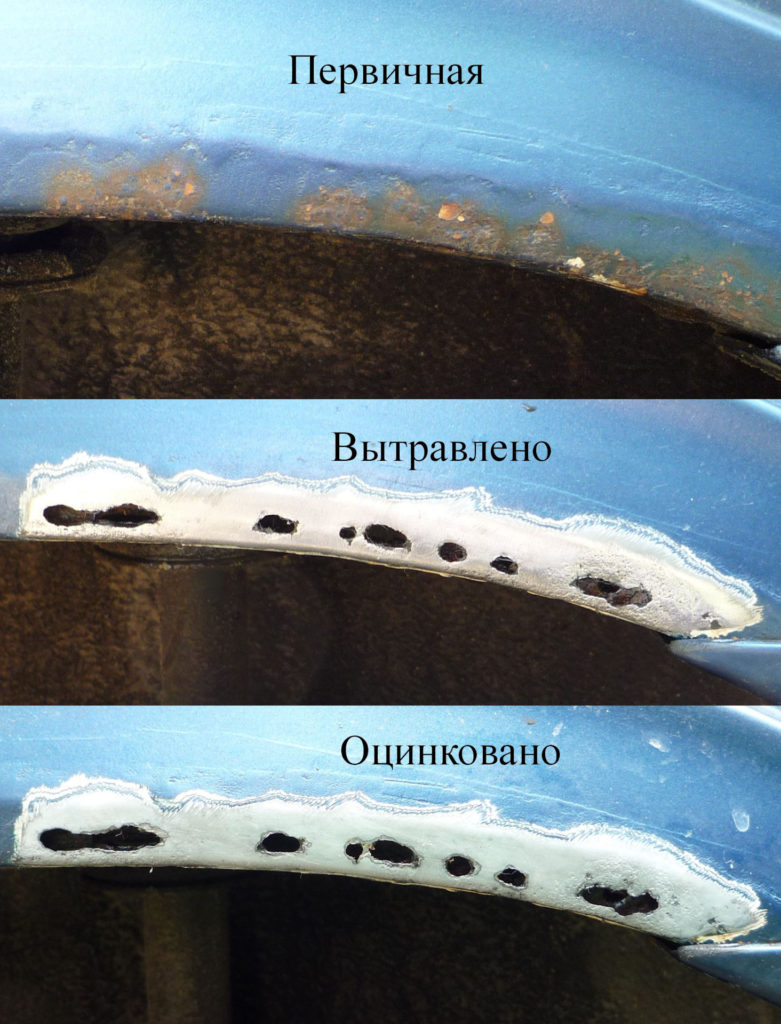
Для начала нужно осуществить зачистку от уже образовавшейся коррозии. Для этого нужно провести манипуляции присущие механическому способу, т.е. нужно зачистить поверхность с помощью скребка или любого другого инструмента. Далее нужно подключить к плюсовой клемме источника тока любой металл меньшей химической активности нежели железо, например, кусок нержавеющей стали.
На поверхность детали, которую необходимо отчистить от ржавчины, наносится кислота. Во время приближения электрода к обработанному кислотой месту, начинается активное образование кислорода, в связи с чем вещество, находящееся на поверхности изделия, начинает бурлить.

Если вы пронаблюдали данную реакцию, значит процесс очистки металла от коррозии запущен. Длительность проведения данной процедуры варьируется в зависимости от степени ржавчины и прочих факторов. По истечении времени, поверхность нужно промыть и подготовить для грунтовки и окраски. Таким образом, удаление коррозии с металлов лучше всего осуществлять с помощью электролиза нежели механического способа.
Есть такой интересный пластилин, называется «автопластилин». Был куплен на пробу как средство удаления ржавчины с металлических поверхностей. Он работает, но подходит для слабой степени загрязнения ржавчиной. Также его используют для герметизации щелей и кузовных дыр до 4-5см в диаметре, а также как антикор и виброизолятор.

